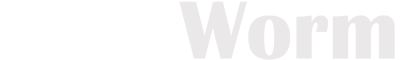Damıtma, iki veya daha fazla bileşen içeren bir karışımın ısıtılıp, buhar ve sıvı faz oluşturmak suretiyle daha uçucu bileşence zengin karışımların elde edilmesini sağlayan ayırma işlemidir. Distilasyon işlemi sırasında, buhar faz daha uçucu olan A bileşeni tarafından zenginleşirken, sıvı faz ise kaynama sıcaklığı daha yüksek olan B bileşenince zenginleşir. Fakat yüzde 100 A içeren bir buhar faz elde edilemez.
Diğer bir tanımlama ile; tüm bileşenlerinin uçucu olmak zorunda olduğu, yüksek oranlarda ayırmaya izin veren bir çeşit ayırma prosesidir. İki veya daha fazla bileşenli sıvı karışımlarının ısıtılıp buhar ve sıvı faz oluşturulması suretiyle, daha uçucu bileşence zengin karışımların elde edilmesine denir.
Distilasyonun gerçekleştirilebilmesi için temel şart, denge durumuna erişmiş buhar-sıvı sisteminde, buhar fazın sıvı fazdan farklı bileşime sahip olmasıdır. Buhar ve sıvı faz bileşimleri aynı olursa, distilasyonda yeterli bir ayırma gerçekleşmez.
Damıtma, özellikle organik bileşiklerin saflaştırılması ve ayrılmasında en çok kullanılan yöntemlerden biridir. Kaynama noktasında bulunan bir sıvıya daha fazla ısı verilirse sıvının sıcaklığı artmaz, verilen ısı sıvının buhar haline dönüşmesini sağlar. Sıcaklık, sıvının tamamen buhar halinde uzaklaşmasına kadar sabit kalır. Bu yöntemle buhar basınçları farklı olan sıvılar birbiriniden ayrılabilir.
Çeşitli parametreler göz önüne alınarak distilasyon çeşitlerinin sınıflandırılması mümkündür. Çalışma şekline göre sürekli-kesikli; besleme akımına göre ikili sistem-çoklu sistem; alınan ürün akımının sayısına göre tek akım-çok akım; ayırma işleminde ek besleme akımı kullanılıp kullanılmamasına göre azeotropik-ekstraktif-tuz katkılı; kolon iç yapısına göre raflı kolon-dolgulu kolon gibi sınıflandırmalar mümkündür. Ayrıca riflaks varlığına göre de sınıflandırma söz konusudur.
Damıtma Türleri Nelerdir?
Normal Atmosfer Basıncında Yapılan Destilasyon Türleri
1- Normal Destilayon: Kaynama sıcaklığına yakın sıcaklıklarda bozunmayan maddelere uygulanır.
2- Fraksiyonlu Destilayon: Kaynama noktaları birbirine yakın maddelerin ayrılmasında kullanılır.
3- Su buharı Destilayon: Suda çözünmeyen ve miktarı az olan maddeleri uçucu olmayan karışımlardan ayırmak için özellikle madde 100 oC nin üzerinde kaynıyorsa ve kaynama noktasına yakın sıcaklıklarda bozunuyorsa su buharı destilasyonu kullanılır. Kaynama sıcaklıklarının altında bozunabilen maddeler için de kullanılır.
4- Kuru Destilayon: Katı maddelerin ısı etkisiyle parçalanıp distile edilebilir maddeler vermesi ve bunların distile edilmesi esasına dayanır.En büyük sakıncası katı maddelerin ısıyı iyi iletmemesi ve parçalanma sonucu istenmeyen ürünlerin de oluşmasıdır.çalışma şekli normal distilasyonda olduğu gibidir.Ayırma ve saflaştırmadan çok sentez tekniği ( örneğin keton sentezi ) olarak önem taşır.
Normal Atmosfer Basıncından Düşük Basınçlarda Yapılan Destilasyon Türü
Vakum Destilayon: Kaynama sıcaklıklarının altında bozunabilen maddeler için kullanılır.